cho 20g X gồm CuO và Fe2O3 tác dụng hết với 200ml Hcl 3,5M
a tìm thành phần % theo khối lượng 2 oxi trong hh , b tìm nồng độ % của đ thu được c tìm nồng độ % của đ thu đc biết DddHcl là 0,8 g/ml
Những câu hỏi liên quan
Cho 20 gam hỗn hợp X gồm CuO và
F
e
2
O
3
tác dụng vừa đủ với 0,2 lít dung dịch HCl có nồng độ 3,5M. Thành phần phần trăm theo khối lượng của CuO và
F
e
2
O
3
trong hỗn hợp X lần lượt là : A. 25% và 75% B. 20% và 80% C. 22% và 78% D. 30% và 70%
Đọc tiếp
Cho 20 gam hỗn hợp X gồm CuO và F e 2 O 3 tác dụng vừa đủ với 0,2 lít dung dịch HCl có nồng độ 3,5M. Thành phần phần trăm theo khối lượng của CuO và F e 2 O 3 trong hỗn hợp X lần lượt là :
A. 25% và 75%
B. 20% và 80%
C. 22% và 78%
D. 30% và 70%
Chọn B
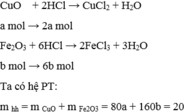
Gọi a là số mol của CuO và b là số mol của F e 2 O 3 có trong 20 gam
hh 200 ml dd HCl 3,5 M => nHCl = 0,2 . 3,5 = 0,7 mol
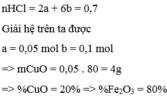
Đúng 0
Bình luận (0)
3.10 gam hh CuO và NaOH tác dụng hết với 200ml dd HCl thu đc 16,5 g muối.
a. Tính % khối lượng các chất có trong hh đầu.
b. Tính nồng độ mol HCl cần dùng.
a,
PTHH: CuO + 2HCl → CuCl2 + H2
Mol: x x
PTHH: NaOH + HCl → NaCl + H2O
Mol: y y
Ta có:\(\left\{{}\begin{matrix}80x+40y=10\\135x+58,5y=16,5\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,104\\y=0,042\end{matrix}\right.\)
PTHH: CuO + 2HCl → CuCl2 + H2
Mol: 0,104 0,208
PTHH: NaOH + HCl → NaCl + H2O
Mol: 0,042 0,042
\(\Rightarrow\%m_{CuO}=\dfrac{0,104.80.100}{10}=83,2\%;\%m_{NaOH}=100\%-83,2\%=16,8\%\)
b,\(n_{HCl}=0,208+0,042=0,25\left(mol\right)\)
\(\Rightarrow C_{M_{ddHCl}}=\dfrac{0,25}{0,2}=1,25M\)
Đúng 2
Bình luận (0)
1) 10 gam hh CuO và NaOH tác dụng hết với 200ml dd HCl thu đc 16,5 g muối.
a. Tính % khối lượng các chất có trong hh đầu.
b. Tính nồng độ mol HCl cần dùng.
Cho 27,4g hỗn hợp gồm Na2O và Na2CO3 tác dụng hết với 200ml dung dịch HCl,khí thu được dẫn qua bình đựng nước vôi trong dư,thấy tạo thành 20g kết tủa,Hãy tính: a)Thàng phần % theo khối lượng mỗi chất trong hôn hợp ban đầu? b)Tính nồng độ mol của dung dịch axit đã dùng?
Cho 10g hh gồm Fe và CuO tác dụng với 200ml dd HCl, thu đc 33,36l khí H2 (đktc)
a) Tính khối lượng từng chất trong hh ban đầu
b) Tính nồng độ mol của dd HCl đã dùng
\(Fe+2HCl\rightarrow FeCl2+H2\)(1)
1____2________1_______1
\(CuO+2HCl\rightarrow CuCl2+H2O\)(2)
1_______2__________1_____1
Ta có :\(n_{H2}=\frac{3,36}{22,4}=0,15\left(mol\right)\)
\(n_{Fe}=\frac{0,15.1}{1}=0,15\left(mol\right)\)
\(\rightarrow m_{Fe}=0,15.56=8,4g\)
\(\rightarrow m_{CuO}=10-8,4=1,6g\)
b,Theo PT(1)\(n_{HCl}=\frac{0,15.2}{1}=0,3\left(mol\right)\)
\(\rightarrow n_{CuO}=\frac{1,6}{80}=0,02\left(mol\right)\)
Theo PT(2)\(n_{HCl}=\frac{0,02.2}{1}=0,04\left(mol\right)\)
\(\rightarrow\Sigma n_{HCl}=0,3+0,04=0,34\left(mol\right)\)
\(\rightarrow CM_{HCl}=\frac{0,34}{0,2}=1,7M\)
Cho 24,4 g hỗn hợp gồm Fe2O3, Fe tác dụng vừa đủ với 200ml dung dịch axit sunfuric (d=1,2/ml) thu được 3,36 lít khí (đktc), dung dịch Y, tính:
a. Thành phần phần trăm theo khối lượng của mỗi chất trong hỗn hợp đầu?
b. Nồng độ mol dung dịch axit sunfuric đã dùng và nồng độ phần trăm các chất có trong dung dịch Y?
giúp mik mấy bài này với ạ
Bài 12: Hòa tan hết 39,2g hh gồm Fe2O3 và Mg trong 260g dd HCI 35,04% (D1,04g/ml ), sau pư thu được dd A có khổi lượng giảm so với tổng ban đầu là 0,6g. Tính nồng độ mọl mỗi chất tan trong dd A. Bài 13: Hòa tan hết 78,4g hh gồm Fe,O, và CuO trong 500g dd HCl 39,2%, sau pư thu dược dd A có nồng độ của FeSO, là 5,256% . al Tính khối lượng mỗi chất trong hh ban đầu. b/ Tính nồng độ phần trăm mỗi chất tan trong dd A. Bài 14: Cho 16,6g hh gồm Al và Fe tan hêết trong 200ml...
Đọc tiếp
giúp mik mấy bài này với ạ
Bài 12: Hòa tan hết 39,2g hh gồm Fe2O3 và Mg trong 260g dd HCI 35,04% (D=1,04g/ml ), sau pư thu được dd A có khổi lượng giảm so với tổng ban đầu là 0,6g. Tính nồng độ mọl mỗi chất tan trong dd A. Bài 13: Hòa tan hết 78,4g hh gồm Fe,O, và CuO trong 500g dd HCl 39,2%, sau pư thu dược dd A có nồng độ của FeSO, là 5,256% . al Tính khối lượng mỗi chất trong hh ban đầu. b/ Tính nồng độ phần trăm mỗi chất tan trong dd A. Bài 14: Cho 16,6g hh gồm Al và Fe tan hêết trong 200ml dd H2SO, 3,5M thu duợc một dd có nồng độ mol cùa muối sắt gấp 2 lần nồng độ của muối nhôm. a/ Tinh khối lượng mỗi chất trong hh ban đầu. b/ Tinh nổng độ mol mỗi chất tan trong dd sau pu. Bài 15: Cho một hh gồm 0,15 mol sắt và 0,1 mol săt(III) oxit vào 182,5g dd HCl 20% Thu được dd A. Cho dd A pu với 192g dd NaOH 25% thu được dd B. a/ Viết PTHH. b/ Tính nồng độ % mỗi chất tan trong dd B. c/ Tính nông độ mol mỗi chất tan trong dd B. Biết DddHCI = 1014g/ml: Ddd)inOU 1 1204
cho 20 gam hổn hợp X gồm cuo và fe2o3 tác dụng vừa đủ với 0,2l dd hcl có nồng đọ 3,5M. Thành phần phần trăm theo khối lượng của cuo và fe2o3 trong hỗn hợp x lần lượt là:
a 30% và 70%
b 20% và 80%
c 22% và 78%
d 25% và 75%
b) 20 % và 80%
Gọi \(n_{CuO} và n_{Fe_2O_3} là x y\)
\(\begin{cases} 80x + 160y= 20\\ 2x+ 6y= 0,2 . 3,5=0,7 \end{cases} \)
x=0,05
y= 0,1
%\(m_{CuO}= \dfrac{0,05 . 80}{20} . 100\)%= 20%
=> %m\(Fe_2O_3\)= 80%
Đúng 0
Bình luận (0)
1. Cho 13g kẽm tác dụng với dung dịch axit sunfuric có nồng độ 20%.
a) Viết PTHH
b) Tính khối lượng dung dịch axit cần dùng
c) Tính thể tích khí thoát ra ở đktc
2. Cho 24g Fe2O3 vào 200ml dd H2SO4 2,5M.
a) Tính khối lượng muối thu đc
b) Tính nồng độ mol dd thu đc sau phản ứng, biết thể tích dd thay đổi ko đáng kể.
3. 200ml dd HCl có nồng độ mol 3,5M hòa tan vừa hết 20 gam hỗn hợp CuO và Fe2O3.
a) Viết PTHH
b) Tính khối lượng mỗi oxit trong hỗn hợp ban đầu
Đọc tiếp
1. Cho 13g kẽm tác dụng với dung dịch axit sunfuric có nồng độ 20%.
a) Viết PTHH
b) Tính khối lượng dung dịch axit cần dùng
c) Tính thể tích khí thoát ra ở đktc
2. Cho 24g Fe2O3 vào 200ml dd H2SO4 2,5M.
a) Tính khối lượng muối thu đc
b) Tính nồng độ mol dd thu đc sau phản ứng, biết thể tích dd thay đổi ko đáng kể.
3. 200ml dd HCl có nồng độ mol 3,5M hòa tan vừa hết 20 gam hỗn hợp CuO và Fe2O3.
a) Viết PTHH
b) Tính khối lượng mỗi oxit trong hỗn hợp ban đầu
PTHH.Zn+ H2SO4 -> ZnSO4 + H2
Theo bài ra ta có: nZn = 13/65 = 0,2 mol
Theo pthh và bài ta có:
+) nH2SO4 = nZn = 0,2 mol
=> mH2SO4 = 0,2 . 98 = 19,6 g
=> mdd H2SO4 = (19,6 . 100%) : 20% = 98%
+)nH2 = nZn = 0,2 mol
=> VH2 = 0,2 . 22,4 = 4,48 l
Vậy...
Đúng 0
Bình luận (0)
2) PTHH: Fe2O3 + 3H2SO4 -> Fe2(SO4)3 + 3H2O
Theo bài ra ta có: nFe2O3 = 24/160 = 0,15 mol
nH2SO4 = 2,5 . 0,2 = 0,5 mol
Theo pthh ta có: nFe2O3 pt = 1 mol ; nH2SO4 pt = 3 mol
Ta có tỉ lệ:
\(\dfrac{nFe2O3\left(bđ\right)}{nFe2O3\left(pt\right)}=\dfrac{0,15}{1}=0,15\)< \(\dfrac{nH2SO4\left(bđ\right)}{nH2SO4\left(pt\right)}=\dfrac{0,5}{3}=0,16\)
=> Sau pư, Fe2O3 tg pư hết , H2SO4 còn dư
Theo pthh và bài ta có:
+nFe2(SO4)3 = nFe2O3 = 0,15 mol
=>mFe2(SO4)3 = 0,15 . 400 = 60 g
CM dd Fe2(SO4)3 = \(\dfrac{0,15}{0,2}=0,75\)(M)
+nH2SO4 tg pư = 3. nFe2O3 = 3. 0,15 = 0,45 mol
=> nH2SO4 dư = 0,5 - 0,45 = 0,05 mol
=> CM dd H2SO4 dư = \(\dfrac{0,05}{0,2}=0,25\left(M\right)\)
Vậy....
Đúng 0
Bình luận (0)



















